摘要:研究發(fā)現(xiàn)現(xiàn)有的HIV藥物可以抑制HTLV-1病毒在小鼠體內(nèi)的傳播。
全球約有1000萬(wàn)人感染危及生命的HTLV-1病毒。然而,人們對(duì)該疾病的了解仍然有限,目前尚無(wú)預(yù)防性治療方法和治愈方法。
但由澳大利亞研究人員共同領(lǐng)導(dǎo)的一項(xiàng)具有里程碑意義的研究可能會(huì)改變這一狀況,因?yàn)樗麄儼l(fā)現(xiàn)現(xiàn)有的 HIV 藥物可以抑制小鼠體內(nèi) HTLV-1 病毒的傳播。
這項(xiàng)研究發(fā)表在《細(xì)胞》雜志上,可能有助于開(kāi)發(fā)出第一種治療方法來(lái)防止這種病毒的傳播,這種病毒在世界各地的許多原住民社區(qū)(包括澳大利亞中部)中流行。
WEHI 和彼得·多爾蒂感染與免疫研究所(多爾蒂研究所)的研究還確定了一種新的藥物靶點(diǎn),可以消除已感染者的 HTLV-1 陽(yáng)性細(xì)胞,并防止病情進(jìn)展。

圖1 體內(nèi)實(shí)驗(yàn)表明:聯(lián)合抗逆轉(zhuǎn)錄病毒療法與MCL-1抑制可緩解HTLV-1感染
研究摘要:
由 WEHI 和多爾蒂研究所共同領(lǐng)導(dǎo)的新研究可能帶來(lái)首個(gè)針對(duì) HTLV-1 的預(yù)防性治療,HTLV-1 是世界上最復(fù)雜且最被忽視的病毒之一。
研究發(fā)現(xiàn),目前市場(chǎng)上已有的兩種特定的抗艾滋病毒藥物可以抑制人源化小鼠體內(nèi) HTLV-1 的傳播并預(yù)防疾病,從而確定了第一種針對(duì) HTLV-1 的預(yù)防性治療方法。
其次,當(dāng) HIV 抗病毒藥物與誘導(dǎo)細(xì)胞死亡的化合物結(jié)合使用時(shí),受感染的細(xì)胞就會(huì)被殺死——這標(biāo)志著未來(lái)該疾病的潛在治療策略。
這一前所未有的發(fā)現(xiàn)可能使這些藥物能夠進(jìn)入臨床試驗(yàn),阻止 HTLV-1 致病水平的形成。
人類 T 細(xì)胞白血病病毒 1 型 (HTLV-1) 是一種感染與 HIV 相同細(xì)胞類型的病毒——T 細(xì)胞,T 細(xì)胞是一種幫助身體抵抗感染的血液免疫細(xì)胞。
一小部分感染HTLV-1的人在長(zhǎng)期感染后會(huì)患上嚴(yán)重疾病,例如成人T細(xì)胞白血病和脊髓炎癥。
聯(lián)合主要作者兼 WEHI 實(shí)驗(yàn)室負(fù)責(zé)人 Marcel Doerflinger 博士表示,這項(xiàng)新研究的成果令人鼓舞,可能有助于找到針對(duì)世界上最被忽視的病毒之一的急需的治療和預(yù)防策略。
Doerflinger博士說(shuō):“我們的研究標(biāo)志著研究小組首次能夠在生物體內(nèi)抑制這種病毒。”
“由于 HTLV-1 癥狀可能需要數(shù)十年才會(huì)出現(xiàn),因此當(dāng)人們知道自己感染時(shí),免疫損傷已經(jīng)全面展開(kāi)。
“抑制病毒的傳播使我們能夠在病毒對(duì)免疫功能造成不可逆轉(zhuǎn)的損害,導(dǎo)致疾病和過(guò)早死亡之前阻止它。”
經(jīng)過(guò)10年的研究,合作團(tuán)隊(duì)分離出了這種病毒,并開(kāi)發(fā)了世界上第一個(gè)HTLV-1人源化小鼠模型,使他們能夠研究這種病毒在具有類似人類免疫系統(tǒng)的生物體中的行為。
這些小鼠被移植了易受HTLV-1感染的人類免疫細(xì)胞,其中包括澳大利亞基因型新穎的HTLV-1毒株。國(guó)際毒株和澳大利亞毒株在這些人類免疫系統(tǒng)小鼠中同樣引發(fā)了白血病和炎癥性肺病。
隨后,研究人員給小鼠注射了替諾福韋和多替拉韋—— 這兩種抗病毒藥物目前已被批準(zhǔn)用于抑制HIV病毒并預(yù)防艾滋病。研究小組發(fā)現(xiàn),這兩種藥物也能有效抑制HTLV-1。
Doerflinger 博士說(shuō):“最令人興奮的是,這些抗病毒藥物已經(jīng)在數(shù)百萬(wàn)艾滋病患者身上使用,這意味著我們的研究成果可以直接應(yīng)用于臨床。”
“我們無(wú)需從頭開(kāi)始,因?yàn)槲覀円呀?jīng)知道這些藥物安全有效。現(xiàn)在我們已經(jīng)證明,它們的用途很可能擴(kuò)展到HTLV-1。”
另一項(xiàng)令人矚目的發(fā)現(xiàn)是,研究小組發(fā)現(xiàn),當(dāng)用 HIV 藥物聯(lián)合另一種抑制已知可幫助流氓細(xì)胞存活的蛋白質(zhì) (MCL-1) 的療法治療小鼠時(shí),可以選擇性地殺死含有 HTLV-1 的人類細(xì)胞。
該團(tuán)隊(duì)目前正在利用精準(zhǔn)的 RNA 療法開(kāi)發(fā)針對(duì) MCL-1 的新方法并建立可進(jìn)行臨床測(cè)試的聯(lián)合治療方法,他們相信這可能為 HTLV-1 提供一種有希望的治療策略。
關(guān)鍵見(jiàn)解
WEHI 這項(xiàng)研究的核心人源化小鼠模型的開(kāi)發(fā)由第一作者 James Cooney 博士和研究主要作者、WEHI 榮譽(yù)研究員兼百年研究所執(zhí)行董事 Marc Pellegrini 教授牽頭。
Pellegrini教授表示,小鼠模型不僅對(duì)于確定潛在的治療靶點(diǎn)至關(guān)重要,還能幫助研究人員了解不同HTLV-1病毒株如何改變疾病癥狀和預(yù)后。這對(duì)于澳大利亞存在的獨(dú)特病毒株HTLV-1c尤為重要。
“長(zhǎng)期以來(lái),人們一直假設(shè)病毒亞型的差異可能會(huì)影響疾病的結(jié)果,但是缺乏對(duì)HTLV-1的研究使得我們很難找到支持這一說(shuō)法所需的證據(jù)——直到現(xiàn)在。”
“我們的研究提供了重要的見(jiàn)解,使我們能夠更好地了解影響我們第一民族社區(qū)的病毒的獨(dú)特分子組成的后果。這將進(jìn)一步幫助我們研究創(chuàng)造控制這種病毒亞型傳播所需工具的方法。”
開(kāi)發(fā)小鼠模型所需的人類HTLV-1樣本是通過(guò)Doherty研究所的臨床科學(xué)家和傳染病醫(yī)師Lloyd einsedel副教授的一線臨床工作獲得的,他為澳大利亞中部提供了十多年的臨床服務(wù),并致力于將HTLV-1放在地圖上。
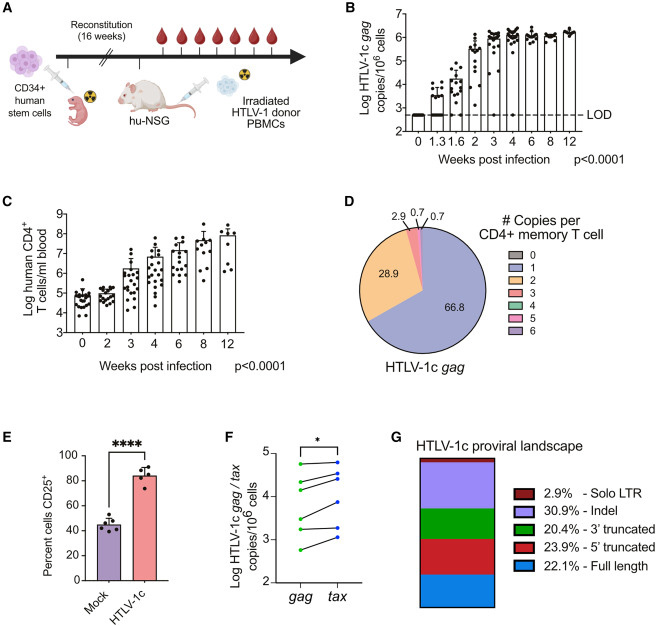
圖2 感染HTLV-1c亞型的人源化小鼠發(fā)生的疾病與人類感染特征相符
一種被忽視的疾病
多爾蒂研究所分子病毒學(xué)負(fù)責(zé)人、該研究的共同主要作者、墨爾本大學(xué)教授Damian Purcell從第一民族捐贈(zèng)者身上分離出了這種病毒,并發(fā)現(xiàn)了來(lái)自澳大利亞中部的HTLV-1c毒株與國(guó)際上發(fā)現(xiàn)的HTLV-1a毒株之間的顯著遺傳差異。
新的研究結(jié)果表明,兩種HTLV-1菌株都會(huì)在小鼠中引起疾病,而HTLV-1c表現(xiàn)出更具攻擊性的特征。已確定的藥物治療方法對(duì)這兩種菌株同樣有效。
Purcell教授和Lloyd einsedel副教授多年來(lái)與全國(guó)土著社區(qū)控制衛(wèi)生組織(NACCHO) HTLV-1委員會(huì)和澳大利亞衛(wèi)生部合作,倡導(dǎo)世界衛(wèi)生組織(WHO)對(duì)HTLV-1的指導(dǎo),使他們?cè)?021年正式將該病毒歸類為對(duì)人類有威脅的病原體。
這導(dǎo)致世衛(wèi)組織制定了正式的政策,以減少國(guó)際傳播,并在澳大利亞中部國(guó)家艾滋病防治中心的領(lǐng)導(dǎo)下制定了HTLV-1c臨床管理指南。
Purcell教授說(shuō):“盡管澳大利亞的HTLV-1負(fù)擔(dān)很高,但這種病毒及其相關(guān)疾病在大多數(shù)州仍未得到通報(bào),該國(guó)的真實(shí)感染率仍不得而知。”
“有HTLV-1風(fēng)險(xiǎn)的人應(yīng)該得到生物醫(yī)學(xué)工具,比如那些為其他血液傳播的持續(xù)性病毒感染(如艾滋病毒)提供改變游戲規(guī)則的治療和預(yù)防選擇的生物醫(yī)學(xué)工具。
“這是一個(gè)真正的機(jī)會(huì)來(lái)防止HTLV-1的傳播,并結(jié)束由這些感染引起的疾病。我們的研究結(jié)果是這方面的重大飛躍。”
該研究小組目前正在與在這項(xiàng)研究中使用HIV抗病毒藥物的公司進(jìn)行談判,以確定HTLV-1患者是否可以納入他們正在進(jìn)行的臨床試驗(yàn)。如果成功,這將為這些藥物成為第一個(gè)被批準(zhǔn)的針對(duì)HTLV-1獲得的暴露前預(yù)防藥物鋪平道路。
這些發(fā)現(xiàn)得到了澳大利亞艾滋病和肝炎病毒學(xué)研究中心、菲利斯康納紀(jì)念信托基金、德拉肯斯堡信托基金和國(guó)家衛(wèi)生和醫(yī)學(xué)研究委員會(huì) (NHMRC) 的支持。
參考資料
[1] Combination antiretroviral therapy and MCL-1 inhibition mitigate HTLV-1 infection in vivo
摘要:研究發(fā)現(xiàn)現(xiàn)有的HIV藥物可以抑制HTLV-1病毒在小鼠體內(nèi)的傳播。
全球約有1000萬(wàn)人感染危及生命的HTLV-1病毒。然而,人們對(duì)該疾病的了解仍然有限,目前尚無(wú)預(yù)防性治療方法和治愈方法。
但由澳大利亞研究人員共同領(lǐng)導(dǎo)的一項(xiàng)具有里程碑意義的研究可能會(huì)改變這一狀況,因?yàn)樗麄儼l(fā)現(xiàn)現(xiàn)有的 HIV 藥物可以抑制小鼠體內(nèi) HTLV-1 病毒的傳播。
這項(xiàng)研究發(fā)表在《細(xì)胞》雜志上,可能有助于開(kāi)發(fā)出第一種治療方法來(lái)防止這種病毒的傳播,這種病毒在世界各地的許多原住民社區(qū)(包括澳大利亞中部)中流行。
WEHI 和彼得·多爾蒂感染與免疫研究所(多爾蒂研究所)的研究還確定了一種新的藥物靶點(diǎn),可以消除已感染者的 HTLV-1 陽(yáng)性細(xì)胞,并防止病情進(jìn)展。

圖1 體內(nèi)實(shí)驗(yàn)表明:聯(lián)合抗逆轉(zhuǎn)錄病毒療法與MCL-1抑制可緩解HTLV-1感染
研究摘要:
由 WEHI 和多爾蒂研究所共同領(lǐng)導(dǎo)的新研究可能帶來(lái)首個(gè)針對(duì) HTLV-1 的預(yù)防性治療,HTLV-1 是世界上最復(fù)雜且最被忽視的病毒之一。
研究發(fā)現(xiàn),目前市場(chǎng)上已有的兩種特定的抗艾滋病毒藥物可以抑制人源化小鼠體內(nèi) HTLV-1 的傳播并預(yù)防疾病,從而確定了第一種針對(duì) HTLV-1 的預(yù)防性治療方法。
其次,當(dāng) HIV 抗病毒藥物與誘導(dǎo)細(xì)胞死亡的化合物結(jié)合使用時(shí),受感染的細(xì)胞就會(huì)被殺死——這標(biāo)志著未來(lái)該疾病的潛在治療策略。
這一前所未有的發(fā)現(xiàn)可能使這些藥物能夠進(jìn)入臨床試驗(yàn),阻止 HTLV-1 致病水平的形成。
人類 T 細(xì)胞白血病病毒 1 型 (HTLV-1) 是一種感染與 HIV 相同細(xì)胞類型的病毒——T 細(xì)胞,T 細(xì)胞是一種幫助身體抵抗感染的血液免疫細(xì)胞。
一小部分感染HTLV-1的人在長(zhǎng)期感染后會(huì)患上嚴(yán)重疾病,例如成人T細(xì)胞白血病和脊髓炎癥。
聯(lián)合主要作者兼 WEHI 實(shí)驗(yàn)室負(fù)責(zé)人 Marcel Doerflinger 博士表示,這項(xiàng)新研究的成果令人鼓舞,可能有助于找到針對(duì)世界上最被忽視的病毒之一的急需的治療和預(yù)防策略。
Doerflinger博士說(shuō):“我們的研究標(biāo)志著研究小組首次能夠在生物體內(nèi)抑制這種病毒。”
“由于 HTLV-1 癥狀可能需要數(shù)十年才會(huì)出現(xiàn),因此當(dāng)人們知道自己感染時(shí),免疫損傷已經(jīng)全面展開(kāi)。
“抑制病毒的傳播使我們能夠在病毒對(duì)免疫功能造成不可逆轉(zhuǎn)的損害,導(dǎo)致疾病和過(guò)早死亡之前阻止它。”
經(jīng)過(guò)10年的研究,合作團(tuán)隊(duì)分離出了這種病毒,并開(kāi)發(fā)了世界上第一個(gè)HTLV-1人源化小鼠模型,使他們能夠研究這種病毒在具有類似人類免疫系統(tǒng)的生物體中的行為。
這些小鼠被移植了易受HTLV-1感染的人類免疫細(xì)胞,其中包括澳大利亞基因型新穎的HTLV-1毒株。國(guó)際毒株和澳大利亞毒株在這些人類免疫系統(tǒng)小鼠中同樣引發(fā)了白血病和炎癥性肺病。
隨后,研究人員給小鼠注射了替諾福韋和多替拉韋—— 這兩種抗病毒藥物目前已被批準(zhǔn)用于抑制HIV病毒并預(yù)防艾滋病。研究小組發(fā)現(xiàn),這兩種藥物也能有效抑制HTLV-1。
Doerflinger 博士說(shuō):“最令人興奮的是,這些抗病毒藥物已經(jīng)在數(shù)百萬(wàn)艾滋病患者身上使用,這意味著我們的研究成果可以直接應(yīng)用于臨床。”
“我們無(wú)需從頭開(kāi)始,因?yàn)槲覀円呀?jīng)知道這些藥物安全有效。現(xiàn)在我們已經(jīng)證明,它們的用途很可能擴(kuò)展到HTLV-1。”
另一項(xiàng)令人矚目的發(fā)現(xiàn)是,研究小組發(fā)現(xiàn),當(dāng)用 HIV 藥物聯(lián)合另一種抑制已知可幫助流氓細(xì)胞存活的蛋白質(zhì) (MCL-1) 的療法治療小鼠時(shí),可以選擇性地殺死含有 HTLV-1 的人類細(xì)胞。
該團(tuán)隊(duì)目前正在利用精準(zhǔn)的 RNA 療法開(kāi)發(fā)針對(duì) MCL-1 的新方法并建立可進(jìn)行臨床測(cè)試的聯(lián)合治療方法,他們相信這可能為 HTLV-1 提供一種有希望的治療策略。
關(guān)鍵見(jiàn)解
WEHI 這項(xiàng)研究的核心人源化小鼠模型的開(kāi)發(fā)由第一作者 James Cooney 博士和研究主要作者、WEHI 榮譽(yù)研究員兼百年研究所執(zhí)行董事 Marc Pellegrini 教授牽頭。
Pellegrini教授表示,小鼠模型不僅對(duì)于確定潛在的治療靶點(diǎn)至關(guān)重要,還能幫助研究人員了解不同HTLV-1病毒株如何改變疾病癥狀和預(yù)后。這對(duì)于澳大利亞存在的獨(dú)特病毒株HTLV-1c尤為重要。
“長(zhǎng)期以來(lái),人們一直假設(shè)病毒亞型的差異可能會(huì)影響疾病的結(jié)果,但是缺乏對(duì)HTLV-1的研究使得我們很難找到支持這一說(shuō)法所需的證據(jù)——直到現(xiàn)在。”
“我們的研究提供了重要的見(jiàn)解,使我們能夠更好地了解影響我們第一民族社區(qū)的病毒的獨(dú)特分子組成的后果。這將進(jìn)一步幫助我們研究創(chuàng)造控制這種病毒亞型傳播所需工具的方法。”
開(kāi)發(fā)小鼠模型所需的人類HTLV-1樣本是通過(guò)Doherty研究所的臨床科學(xué)家和傳染病醫(yī)師Lloyd einsedel副教授的一線臨床工作獲得的,他為澳大利亞中部提供了十多年的臨床服務(wù),并致力于將HTLV-1放在地圖上。

圖2 感染HTLV-1c亞型的人源化小鼠發(fā)生的疾病與人類感染特征相符
一種被忽視的疾病
多爾蒂研究所分子病毒學(xué)負(fù)責(zé)人、該研究的共同主要作者、墨爾本大學(xué)教授Damian Purcell從第一民族捐贈(zèng)者身上分離出了這種病毒,并發(fā)現(xiàn)了來(lái)自澳大利亞中部的HTLV-1c毒株與國(guó)際上發(fā)現(xiàn)的HTLV-1a毒株之間的顯著遺傳差異。
新的研究結(jié)果表明,兩種HTLV-1菌株都會(huì)在小鼠中引起疾病,而HTLV-1c表現(xiàn)出更具攻擊性的特征。已確定的藥物治療方法對(duì)這兩種菌株同樣有效。
Purcell教授和Lloyd einsedel副教授多年來(lái)與全國(guó)土著社區(qū)控制衛(wèi)生組織(NACCHO) HTLV-1委員會(huì)和澳大利亞衛(wèi)生部合作,倡導(dǎo)世界衛(wèi)生組織(WHO)對(duì)HTLV-1的指導(dǎo),使他們?cè)?021年正式將該病毒歸類為對(duì)人類有威脅的病原體。
這導(dǎo)致世衛(wèi)組織制定了正式的政策,以減少國(guó)際傳播,并在澳大利亞中部國(guó)家艾滋病防治中心的領(lǐng)導(dǎo)下制定了HTLV-1c臨床管理指南。
Purcell教授說(shuō):“盡管澳大利亞的HTLV-1負(fù)擔(dān)很高,但這種病毒及其相關(guān)疾病在大多數(shù)州仍未得到通報(bào),該國(guó)的真實(shí)感染率仍不得而知。”
“有HTLV-1風(fēng)險(xiǎn)的人應(yīng)該得到生物醫(yī)學(xué)工具,比如那些為其他血液傳播的持續(xù)性病毒感染(如艾滋病毒)提供改變游戲規(guī)則的治療和預(yù)防選擇的生物醫(yī)學(xué)工具。
“這是一個(gè)真正的機(jī)會(huì)來(lái)防止HTLV-1的傳播,并結(jié)束由這些感染引起的疾病。我們的研究結(jié)果是這方面的重大飛躍。”
該研究小組目前正在與在這項(xiàng)研究中使用HIV抗病毒藥物的公司進(jìn)行談判,以確定HTLV-1患者是否可以納入他們正在進(jìn)行的臨床試驗(yàn)。如果成功,這將為這些藥物成為第一個(gè)被批準(zhǔn)的針對(duì)HTLV-1獲得的暴露前預(yù)防藥物鋪平道路。
這些發(fā)現(xiàn)得到了澳大利亞艾滋病和肝炎病毒學(xué)研究中心、菲利斯康納紀(jì)念信托基金、德拉肯斯堡信托基金和國(guó)家衛(wèi)生和醫(yī)學(xué)研究委員會(huì) (NHMRC) 的支持。
參考資料
[1] Combination antiretroviral therapy and MCL-1 inhibition mitigate HTLV-1 infection in vivo



