病毒疫苗的研發與生產是一場與時間賽跑的科技戰役,而其核心與瓶頸在于大規模、高效、穩定的細胞培養和病毒擴增工藝。在病毒疫苗生產中,細胞是病毒復制的 “宿主工廠”,細胞培養工藝的優劣直接決定后續病毒擴增效率。從傳統的雞胚、原代細胞到如今廣泛應用的連續傳代細胞系(如Vero、MDCK細胞),細胞基質的選擇直接影響病毒的適配性和擴增能力)。優化方向包括尋找更高效、更安全、無動物源成分的細胞培養體系。
西寶生物科技(上海)是一家專注于生命科學和生物技術領域的高科技企業,其業務覆蓋了從研發到生產的多個環節。在病毒疫苗領域,西寶生物并非直接從事成品疫苗的開發和生產,而是定位于關鍵的上游供應商和技術服務伙伴,為疫苗研發和生產機構(如CXO企業、生物制藥公司、科研院所)提供核心原材料、試劑、技術平臺及解決方案。
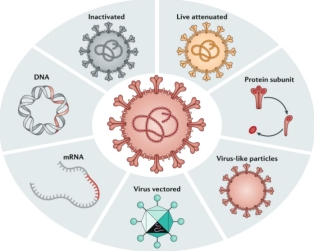
病毒疫苗類型
一、 主要病毒疫苗技術平臺
1. 滅活疫苗 (Inactivated Virus Vaccine)
滅活疫苗是通過物理或化學方法將病毒滅活后制成的疫苗,是最成熟的疫苗開發技術。目前已成功研發并廣泛使用的產品包括甲肝滅活疫苗、手足口病滅活疫苗、脊髓灰質炎滅活疫苗等。
優點:技術成熟、可利用現有生產條件快速開發、穩定性好、安全性高(無復制能力)。
挑戰:免疫原性相對較弱,通常需要佐劑并多次接種;誘導的細胞免疫反應較弱;可能存在抗體依賴性增強(ADE)效應的風險。
2. 減毒活疫苗 (Live Attenuated Vaccine)
減毒活疫苗是通過一定方式處理病毒,獲得毒力減弱的毒株后制成的疫苗。目前廣泛使用的麻疹疫苗就是減毒活疫苗。
優點:通常能誘導強烈的、持久的體液免疫和細胞免疫,模擬自然感染過程,保護效果通常很好。
挑戰:對于免疫力低下的人群可能存在致病風險;有毒力回復的極小可能性;通常需要冷藏,運輸儲存要求較高。
3. 亞單位疫苗/重組蛋白疫苗 (Subunit Vaccine)
亞單位疫苗是利用基因工程技術,生產病毒中最可能作為抗原的蛋白亞單位制成的疫苗。目前已成功研發的產品包括乙肝疫苗、宮頸癌(HPV)疫苗等。
優點:成分明確,安全性高,研發工藝成熟,可大規模生產。
挑戰:免疫原性較弱,需要佐劑和多次接種;激活CD8+ T細胞免疫的效果弱;若使用鋁佐劑,免疫反應可能偏向Th2型,不適合呼吸道黏膜接種。
4. 病毒樣顆粒疫苗 (Virus-Like Particle Vaccine, VLP)
病毒樣顆粒是由多個病毒蛋白自發組裝形成的、在結構上高度模擬真實病毒但缺乏病毒基因組的顆粒。市場上的多種乙肝疫苗和HPV疫苗都屬于VLP疫苗。
優點:具有病毒的高度結構相似性,因此免疫原性很強,能有效誘導高效的中和抗體;不含遺傳物質,非常安全。
挑戰:生產工藝復雜,組裝和純化步驟要求高,成本相對較高。
5. 重組病毒載體疫苗 (Recombinant Viral Vector Vaccine)
該技術利用經過基因工程改造的病毒(如腺病毒)作為載體,攜帶目標病毒抗原的基因。接種后,載體病毒在人體內感染細胞并表達抗原蛋白,從而引發免疫反應。
優點:能誘導強烈的細胞免疫;通常無需佐劑;一些載體(如ChAdOx)可單次接種并提供保護;適合開發黏膜疫苗;生產周期短。
挑戰:若人體已對載體病毒存在預存免疫力,可能會削弱疫苗效果。
6. 核酸疫苗 (Nucleic Acid Vaccine)
包括DNA疫苗和mRNA疫苗。其原理是將編碼病毒抗原的遺傳物質(DNA或mRNA)直接導入人體細胞,利用人體細胞自身的機器來生產抗原蛋白,從而激發免疫反應。mRNA疫苗在新冠疫情期間大放異彩。
優點:
研發速度快:平臺化技術,一旦獲得病原體基因序列即可快速設計疫苗。
安全性高:不含病毒成分,無感染風險。
免疫效果好:能誘導全面的體液免疫和T細胞免疫。
挑戰:mRNA疫苗的脂質納米顆粒(LNP)遞送系統需要低溫儲存;長期安全性數據仍在積累中。
病毒疫苗生產環節
核心生產環節 | 滅活疫苗 | 減毒活疫苗 | 病毒載體疫苗(如腺病毒載體) | 重組蛋白疫苗(如亞單位疫苗) | mRNA 疫苗 | DNA 疫苗 |
1. 病毒種子制備 | 分離、鑒定目標病毒株,在細胞或雞胚中擴增培養 | 分離目標病毒株,通過傳代等方式人工減毒 | 將目標病毒抗原基因插入載體病毒 | 無活病毒參與 | 無活病毒參與 | 無活病毒參與 |
2. 大規模生產抗原 | 在生物反應器(細胞工廠 / 雞胚)中大規模培養活病毒 | 在生物反應器 中大規模培養減毒活病毒 | 在特定細胞系中培養重組載體病毒 | 在工程細胞 (酵母、昆蟲細胞 / 動物細胞) 中表達目標抗原蛋白 | 體外合成目標抗原的 mRNA 序列 | 體外合成編碼目標抗原的 DNA 質粒 |
3. 收獲與初步純化 | 收獲含病毒培養液,離心 / 過濾去除大顆粒雜質 | 收獲含病毒培養液,離心 / 過濾去除大顆粒雜質 | 收獲含病毒載體培養液,離心過濾 | 收獲細胞培養液或裂解液,分離目標蛋白 | 收獲反應液,進行初步純化 | 收獲細菌培養物,提取純化質粒 DNA |
4. 滅活 / 減毒確認識裂 | 使用化學試劑 (甲醛 /β 丙內酯) 徹底滅活病毒活性 | 嚴格檢測確保減毒穩定性和安全性 | 通常不需要額外滅活 | 無活病毒 | 無活病毒 | 無活病毒 |
5. 高度純化 | 超濾和層析等色譜技術去除雜質 (細胞碎片、培養基成分、滅活劑) | 類似滅活疫苗純化 | 類似滅活疫苗純化,去除宿主細胞 DNA / 蛋白 | 多步層析和過濾獲得高純度蛋白 | 去除雜質 (酶、DNA 模板、有機溶劑等),獲得純凈 mRNA | 去除內毒素、宿主雜質等,獲得高純度質粒 |
6. 制劑 | 緩沖液復溶純化病毒,可能添加佐劑 (如鋁佐劑) 增強免疫應答 | 緩沖液復溶純化病毒,通常不加佐劑 | 緩沖液復溶純化病毒載體 | 純化蛋白 + 佐劑 (如鋁佐劑) 混合 | mRNA 包裹入脂質納米顆粒 (LNP),形成保護性遞送系統 | 緩沖液溶解質粒 DNA |
疫苗研究實例
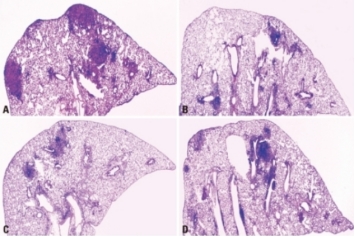
經強毒結核分枝桿菌氣溶膠感染后的肺部組織病理學表現
卡介苗(BCG)可誘導高水平的γ干擾素(IFN-γ),但與單獨接種BCG相比,聯合接種IL-12或IL-18 DNA疫苗構建體與BCG能誘導顯著更高水平的IFN-γ。BCG在結核分枝桿菌感染早期具有高度保護作用,但在感染后期其保護效力會降低。與單獨使用BCG相比,聯合接種IL-12 DNA疫苗構建體與BCG在感染早期保護效果略有增強,在感染后期則顯示出顯著更強的保護效力。
滅活EV71疫苗在SCARB2轉基因小鼠模型中展現交叉保護效力
疫苗接種顯著降低了轉基因小鼠中樞神經系統內的病毒抗原載量;有效緩解了病毒引發的炎癥反應。實驗結果表明,該微載體/生物反應器平臺制備的疫苗具有顯著免疫保護效果,其綜合性能優于傳統轉瓶培養系統。
選擇依據
培養基選擇:Vero細胞培養基適合貼壁培養,MDCK培養基更適合懸浮流感病毒生產。
穩定劑差異:海藻糖適合干燥保存,人血白蛋白用于液態疫苗穩定性提升。
滅活劑對比:β-丙內酯優于甲醛的殘留安全性,Triton X-100需注意環境毒性。
推薦產品
類別 | 產品 | 適用場景 | |
病毒增殖培養基 | VeroSFM | 無血清無動物源,化學成分限定,GMP標準生產,適合大規模工業化疫苗生產 | |
Vero VM (病毒維持液) | 無血清無動物源,支持Vero細胞貼壁培養,適用于狂犬病、乙腦等疫苗生產 | ||
MDCK SFM | 無血清無動物源懸浮培養基,支持MDCK細胞高密度培養,用于流感疫苗生產 | ||
病毒穩定劑 | ACJ1857A | 藥用級海藻糖 | 非還原性穩定劑,保護病毒活性,可常溫保存生物制品 |
ACJ0073B | 蔗糖 | 用于病毒純化密度梯度離心,RNase/DNase Free | |
DCL0119D | 人血白蛋白 | 高濃度白蛋白,作為疫苗穩定劑,防止蛋白變性 | |
病毒滅活試劑 | AJL0175F | β-丙內酯(BPL) | 作用于病毒核酸,滅活時間短,水解產物無毒,適用于狂犬病等疫苗 |
ACH0026Q | Triton X-100 | 非離子去垢劑,破壞脂質膜滅活包膜病毒,適用于生物制品滅活 | |
疫苗佐劑 | AEI0021I | 氫氧化鋁佐劑 | 促進體液免疫(抗體)反應和TH2類細胞免疫反應;用于疫苗和獸用疫苗。 |
參考文獻
[1]. Jeon BY, et al.Co-immunization of plasmid DNA encoding IL-12 and IL-18 with Bacillus Calmette-Guérin vaccine against progressive tuberculosis.Yonsei medical journal(2011)
[2]. Choi HJ, et al. Effect of AcHERV-GmCSF as an Influenza Virus Vaccine Adjuvant. PloS one(2015)
病毒疫苗的研發與生產是一場與時間賽跑的科技戰役,而其核心與瓶頸在于大規模、高效、穩定的細胞培養和病毒擴增工藝。在病毒疫苗生產中,細胞是病毒復制的“宿主工廠”,細胞培養工藝的優劣直接決定后續病毒擴增效率。從傳統的雞胚、原代細胞到如今廣泛應用的連續傳代細胞系(如Vero、MDCK細胞),細胞基質的選擇直接影響病毒的適配性和擴增能力)。優化方向包括尋找更高效、更安全、無動物源成分的細胞培養體系。
西寶生物科技(上海)是一家專注于生命科學和生物技術領域的高科技企業,其業務覆蓋了從研發到生產的多個環節。在病毒疫苗領域,西寶生物并非直接從事成品疫苗的開發和生產,而是定位于關鍵的上游供應商和技術服務伙伴,為疫苗研發和生產機構(如CXO企業、生物制藥公司、科研院所)提供核心原材料、試劑、技術平臺及解決方案。

病毒疫苗類型
一、 主要病毒疫苗技術平臺
1. 滅活疫苗 (Inactivated Virus Vaccine)
滅活疫苗是通過物理或化學方法將病毒滅活后制成的疫苗,是最成熟的疫苗開發技術。目前已成功研發并廣泛使用的產品包括甲肝滅活疫苗、手足口病滅活疫苗、脊髓灰質炎滅活疫苗等。
優點:技術成熟、可利用現有生產條件快速開發、穩定性好、安全性高(無復制能力)。
挑戰:免疫原性相對較弱,通常需要佐劑并多次接種;誘導的細胞免疫反應較弱;可能存在抗體依賴性增強(ADE)效應的風險。
2. 減毒活疫苗 (Live Attenuated Vaccine)
減毒活疫苗是通過一定方式處理病毒,獲得毒力減弱的毒株后制成的疫苗。目前廣泛使用的麻疹疫苗就是減毒活疫苗。
優點:通常能誘導強烈的、持久的體液免疫和細胞免疫,模擬自然感染過程,保護效果通常很好。
挑戰:對于免疫力低下的人群可能存在致病風險;有毒力回復的極小可能性;通常需要冷藏,運輸儲存要求較高。
3. 亞單位疫苗/重組蛋白疫苗 (Subunit Vaccine)
亞單位疫苗是利用基因工程技術,生產病毒中最可能作為抗原的蛋白亞單位制成的疫苗。目前已成功研發的產品包括乙肝疫苗、宮頸癌(HPV)疫苗等。
優點:成分明確,安全性高,研發工藝成熟,可大規模生產。
挑戰:免疫原性較弱,需要佐劑和多次接種;激活CD8+ T細胞免疫的效果弱;若使用鋁佐劑,免疫反應可能偏向Th2型,不適合呼吸道黏膜接種。
4. 病毒樣顆粒疫苗 (Virus-Like Particle Vaccine, VLP)
病毒樣顆粒是由多個病毒蛋白自發組裝形成的、在結構上高度模擬真實病毒但缺乏病毒基因組的顆粒。市場上的多種乙肝疫苗和HPV疫苗都屬于VLP疫苗。
優點:具有病毒的高度結構相似性,因此免疫原性很強,能有效誘導高效的中和抗體;不含遺傳物質,非常安全。
挑戰:生產工藝復雜,組裝和純化步驟要求高,成本相對較高。
5. 重組病毒載體疫苗 (Recombinant Viral Vector Vaccine)
該技術利用經過基因工程改造的病毒(如腺病毒)作為載體,攜帶目標病毒抗原的基因。接種后,載體病毒在人體內感染細胞并表達抗原蛋白,從而引發免疫反應。
優點:能誘導強烈的細胞免疫;通常無需佐劑;一些載體(如ChAdOx)可單次接種并提供保護;適合開發黏膜疫苗;生產周期短。
挑戰:若人體已對載體病毒存在預存免疫力,可能會削弱疫苗效果。
6. 核酸疫苗 (Nucleic Acid Vaccine)
包括DNA疫苗和mRNA疫苗。其原理是將編碼病毒抗原的遺傳物質(DNA或mRNA)直接導入人體細胞,利用人體細胞自身的機器來生產抗原蛋白,從而激發免疫反應。mRNA疫苗在新冠疫情期間大放異彩。
優點:
研發速度快:平臺化技術,一旦獲得病原體基因序列即可快速設計疫苗。
安全性高:不含病毒成分,無感染風險。
免疫效果好:能誘導全面的體液免疫和T細胞免疫。
挑戰:mRNA疫苗的脂質納米顆粒(LNP)遞送系統需要低溫儲存;長期安全性數據仍在積累中。
病毒疫苗生產環節
核心生產環節 | 滅活疫苗 | 減毒活疫苗 | 病毒載體疫苗(如腺病毒載體) | 重組蛋白疫苗(如亞單位疫苗) | mRNA 疫苗 | DNA 疫苗 |
1. 病毒種子制備 | 分離、鑒定目標病毒株,在細胞或雞胚中擴增培養 | 分離目標病毒株,通過傳代等方式人工減毒 | 將目標病毒抗原基因插入載體病毒 | 無活病毒參與 | 無活病毒參與 | 無活病毒參與 |
2. 大規模生產抗原 | 在生物反應器(細胞工廠 / 雞胚)中大規模培養活病毒 | 在生物反應器 中大規模培養減毒活病毒 | 在特定細胞系中培養重組載體病毒 | 在工程細胞 (酵母、昆蟲細胞 / 動物細胞) 中表達目標抗原蛋白 | 體外合成目標抗原的 mRNA 序列 | 體外合成編碼目標抗原的 DNA 質粒 |
3. 收獲與初步純化 | 收獲含病毒培養液,離心 / 過濾去除大顆粒雜質 | 收獲含病毒培養液,離心 / 過濾去除大顆粒雜質 | 收獲含病毒載體培養液,離心過濾 | 收獲細胞培養液或裂解液,分離目標蛋白 | 收獲反應液,進行初步純化 | 收獲細菌培養物,提取純化質粒 DNA |
4. 滅活 / 減毒確認識裂 | 使用化學試劑 (甲醛 /β 丙內酯) 徹底滅活病毒活性 | 嚴格檢測確保減毒穩定性和安全性 | 通常不需要額外滅活 | 無活病毒 | 無活病毒 | 無活病毒 |
5. 高度純化 | 超濾和層析等色譜技術去除雜質 (細胞碎片、培養基成分、滅活劑) | 類似滅活疫苗純化 | 類似滅活疫苗純化,去除宿主細胞 DNA / 蛋白 | 多步層析和過濾獲得高純度蛋白 | 去除雜質 (酶、DNA 模板、有機溶劑等),獲得純凈 mRNA | 去除內毒素、宿主雜質等,獲得高純度質粒 |
6. 制劑 | 緩沖液復溶純化病毒,可能添加佐劑 (如鋁佐劑) 增強免疫應答 | 緩沖液復溶純化病毒,通常不加佐劑 | 緩沖液復溶純化病毒載體 | 純化蛋白 + 佐劑 (如鋁佐劑) 混合 | mRNA 包裹入脂質納米顆粒 (LNP),形成保護性遞送系統 | 緩沖液溶解質粒 DNA |
疫苗研究實例

經強毒結核分枝桿菌氣溶膠感染后的肺部組織病理學表現
卡介苗(BCG)可誘導高水平的γ干擾素(IFN-γ),但與單獨接種BCG相比,聯合接種IL-12或IL-18 DNA疫苗構建體與BCG能誘導顯著更高水平的IFN-γ。BCG在結核分枝桿菌感染早期具有高度保護作用,但在感染后期其保護效力會降低。與單獨使用BCG相比,聯合接種IL-12 DNA疫苗構建體與BCG在感染早期保護效果略有增強,在感染后期則顯示出顯著更強的保護效力。

滅活EV71疫苗在SCARB2轉基因小鼠模型中展現交叉保護效力
疫苗接種顯著降低了轉基因小鼠中樞神經系統內的病毒抗原載量;有效緩解了病毒引發的炎癥反應。實驗結果表明,該微載體/生物反應器平臺制備的疫苗具有顯著免疫保護效果,其綜合性能優于傳統轉瓶培養系統。
選擇依據
培養基選擇:Vero細胞培養基適合貼壁培養,MDCK培養基更適合懸浮流感病毒生產。
穩定劑差異:海藻糖適合干燥保存,人血白蛋白用于液態疫苗穩定性提升。
滅活劑對比:β-丙內酯優于甲醛的殘留安全性,Triton X-100需注意環境毒性。
推薦產品
類別 | 產品 | 適用場景 | |
病毒增殖培養基 | VeroSFM | 無血清無動物源,化學成分限定,GMP標準生產,適合大規模工業化疫苗生產 | |
Vero VM (病毒維持液) | 無血清無動物源,支持Vero細胞貼壁培養,適用于狂犬病、乙腦等疫苗生產 | ||
MDCK SFM | 無血清無動物源懸浮培養基,支持MDCK細胞高密度培養,用于流感疫苗生產 | ||
病毒穩定劑 | ACJ1857A | 藥用級海藻糖 | 非還原性穩定劑,保護病毒活性,可常溫保存生物制品 |
ACJ0073B | 蔗糖 | 用于病毒純化密度梯度離心,RNase/DNase Free | |
DCL0119D | 人血白蛋白 | 高濃度白蛋白,作為疫苗穩定劑,防止蛋白變性 | |
病毒滅活試劑 | AJL0175F | β-丙內酯(BPL) | 作用于病毒核酸,滅活時間短,水解產物無毒,適用于狂犬病等疫苗 |
ACH0026Q | Triton X-100 | 非離子去垢劑,破壞脂質膜滅活包膜病毒,適用于生物制品滅活 | |
疫苗佐劑 | AEI0021I | 氫氧化鋁佐劑 | 促進體液免疫(抗體)反應和TH2類細胞免疫反應;用于疫苗和獸用疫苗。 |
參考文獻
[1]. Jeon BY, et al.Co-immunization of plasmid DNA encoding IL-12 and IL-18 with Bacillus Calmette-Guérin vaccine against progressive tuberculosis.Yonsei medical journal(2011)
[2]. Choi HJ, et al. Effect of AcHERV-GmCSF as an Influenza Virus Vaccine Adjuvant. PloS one(2015)



